
Diagrama de Moeller: qué es y para qué sirve su aplicación
Para hablar del Diagrama de Moeller, debemos remontarnos al siglo XIX, siglo en el que tuvo lugar un gran desarrollo de la química como ciencia de estudio. Hubo grandes avances en este campo que hicieron necesaria una teoría que pudiera explicar de manera detallada cómo funcionaba la estructura atómica.
En este contexto, se desarrolló la teoría de los orbitales atómicos, en la que se establece que los electrones permanecen siempre siguiendo una determinada ruta u órbita alrededor del núcleo atómico. Esto quiere decir que si este tiene una mayor cantidad de electrones, tendrá, por lo tanto, una mayor cantidad de orbitales.
Esta teoría recibe el nombre de Regla de Madelung o “Método de la Lluvia” y, dado que, en un principio puede resultar algo confusa o difícil de entender, en este artículo te vamos a explicar su funcionamiento y las aplicaciones que ha tenido desde su formulación.
Qué es el Diagrama de Moeller

Perteneciente al campo de la Física, el diagrama de Moeller es, como su propio nombre indica, un diagrama en el que se representa el orden en que los electrones llenan los orbitales en una estructura atómica. Se compone de 4 columnas que representan los orbitales en sí, con las letras s, p, d y f.
Este diagrama fue creado por Erwin Madelung, un famoso físico procedente de Alemania en 1881, que también es conocido como el creador de la Regla Madelung. El Diagrama de Moeller parte de la regla que ya había creado este físico años atrás con la intención de explicar el orden energético asociado a los orbitales atómicos.
Si quieres saber qué es el diagrama de Moeller, en aspectos generales, es una especie de gráfica en la que se muestra un rango de presión de entre 0,01 bar y 1000 bar y un rango de temperatura de hasta 800ºC y sirven para intentar explicar cómo se comporta el orden energético asociado a los orbitales atómicos presentes en distintos fluidos.
¿Cómo funciona el Diagrama de Moeller?
Por ejemplo, en un Diagrama de Moeller para el agua y vapor, la “fracción de sequedad”, x, da la fracción de masa de agua en forma de gas que se encuentra presente en la zona húmeda, mientras que el resto de la misma son gotas en estado líquido. Así, se explicaría que los primeros orbitales están vinculados a los electrones que tienen menos energía y los últimos están asociados a los electrones de mayor energía que se encuentran en el átomo.
Para elaborar dicho diagrama, debes determinar el número atómico Z del elemento que vas a estudiar. Este número se asocia al número de electrones que se encuentran presentes en un átomo neutro. Una vez hayas realizado esta tarea, debes rellenar este átomo neutro de los electrones en los orbitales, trazando líneas diagonales que apuntan hacia abajo, de izquierda a derecha. Así pues, el relleno se establece partiendo del orbital 1s, teniendo en cuenta que los orbitales funcionan por capas y por subcapas electrónicas, de manera que en la capa “s” los orbitales contienen dos electrones, en la “p”, contienen 6, en los orbitales “d” se alojan 10 electrones y en los orbitales “f”, encontramos 14 electrones en torno al núcleo atómico.
Trascendencia del Diagrama de Moeller
El diagrama de Moeller permite explicar y calcular la configuración electrónica de los átomos de una manera bastante sencilla y visual que se basa en la regla de Madelung. Gracias a él, la química se masificó como ciencia de estudio y se crearon grandes desarrollos tecnológicos que se aplicaron en los años posteriores a su descubrimiento.
La aplicación de este diagrama ha sido, por lo tanto, muy útil en el campo de la ingeniería, para el diseño de las centrales eléctricas y las turbinas de vapor, pero también para el diseño y desarrollo de sistemas de calefacción, refrigeración y compresores y ha tenido aplicaciones prácticas en el campo de la previsión meteorológica.
Para qué sirve la configuración electrónica
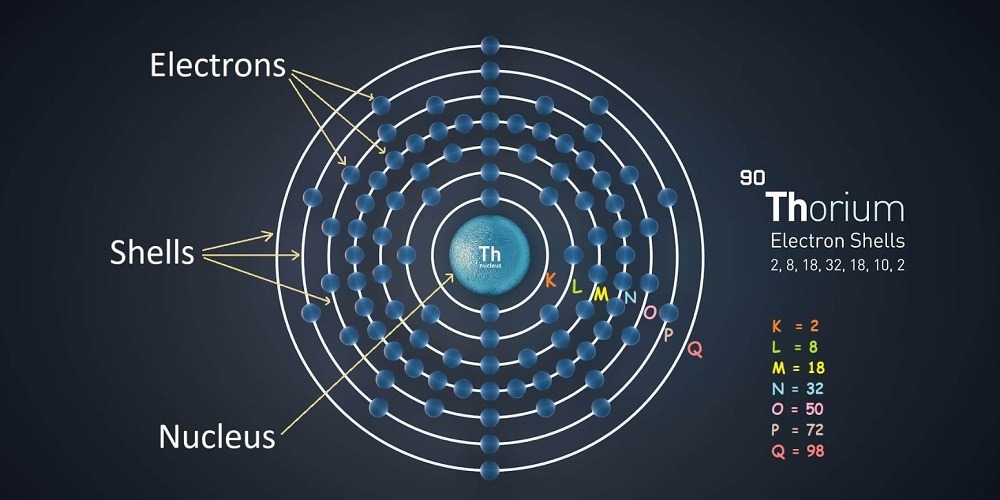
Hemos visto que el Diagrama de Mueller sirve para explicar y calcular la configuración electrónica de los átomos, pero, ¿qué es y para qué sirve la configuración electrónica de los átomos?
La configuración electrónica que podemos ver en el Diagrama de Moeller es la notación estándar que se utiliza para describir la estructura electrónica de los átomos y sus electrones por medio del espacio que estos ocupan en los orbitales de los mismos.
Así, nos permite comprender la forma y la energía de sus electrones, mediante el uso de muchas reglas generales para “asignar la ubicación del electrón” a su estado energético prospectivo, permitiéndonos conocer, pese a la arbitrariedad de sus asignaciones, las capacidades de unión y magnetismo que se desprenden de los propios átomos, así como de otras propiedades de naturaleza química.
Dicho con otras palabras, gracias a la configuración electrónica del Diagrama de Moeller, sabemos qué elementos de la tabla periódica son más fáciles o difíciles de unir y nos permite entender las reacciones químicas de los elementos atendiendo a su naturaleza atómica a nivel de electrones cuando entran en contacto con otras sustancias de naturaleza distinta o les suministramos energía.
Hasta aquí este artículo sobre el Diagrama de Moeller. Esperamos que te haya servido de ayuda y que te haya permitido descubrir el maravilloso mundo de la configuración electrónica de los átomos que forman los elementos del mundo físico y sus distintas aplicaciones prácticas en distintos campos. Recuerda que si necesitas ayuda con tus trabajos de la universidad en Tus Trabajos Universitarios estamos a tu entera disposición.
